Investigadores dirigidos por la Universidad Estatal de Pensilvania han convertido un hongo mortal en un eficaz agente anticancerígeno. Tras aislar una nueva clase de moléculas del Aspergillus flavus, un hongo tóxico de los cereales relacionado con muertes en excavaciones de tumbas antiguas, los investigadores modificaron las sustancias químicas y las probaron en células de leucemia. ¿El resultado? Un prometedor agente anticancerígeno que puede competir con los fármacos aprobados por la FDA y abrir nuevas vías para el descubrimiento de otros medicamentos fúngicos.
A. flavus como fuente inesperada de una nueva y prometedora terapia contra el cáncer
«Los hongos nos dieron la penicilina», afirma Sherry Gao, catedrática asociada de Penn Compact de Ingeniería Química y Biomolecular (CBE) y Bioingeniería (BE) y autora principal de un nuevo estudio en Nature Chemical Biology sobre los hallazgos. «Estos resultados demuestran que se pueden descubrir muchos más fármacos a partir de productos naturales».

Aspergillus flavus, llamado así por sus esporas amarillas, ha sido durante mucho tiempo un culpable microbiano. Después de que los arqueólogos abrieran la tumba del rey Tutankamón en la década de 1920, se produjeron varias muertes prematuras entre los trabajadores de la excavación, lo que alimentó los rumores de que el faraón estaba maldito. Décadas más tarde, los médicos teorizaron que las esporas de hongos que habían permanecido latentes durante miles de años podrían haber desempeñado un papel. En los años setenta, una docena de científicos entraron en la tumba de Casimiro IV, en Polonia. Diez de ellos murieron a las pocas semanas. Investigaciones posteriores revelaron que la tumba contenía A. flavus, cuyas toxinas pueden provocar infecciones pulmonares, sobre todo en personas con sistemas inmunitarios debilitados. Hoy, el mismo hongo es la fuente inesperada de una nueva y prometedora terapia contra el cáncer.
Enfoque innovador
La terapia en cuestión es una clase de péptidos sintetizados ribosómicamente y modificados postraduccionalmente, conocidos como RiPPs, que se pronuncian como la «rasgadura» de un trozo de tela. El nombre hace referencia a la forma en que se produce el compuesto -por el ribosoma, una diminuta estructura celular que fabrica proteínas- y al hecho de que posteriormente se modifica, en este caso para potenciar sus propiedades anticancerígenas.
«Purificar estas sustancias químicas es difícil», explica Qiuyue Nie, investigadora postdoctoral del CBE y primera autora del estudio. Aunque se han identificado miles de RiPP en bacterias, sólo unas pocas se han hallado en hongos. Esto se debe en parte a que investigadores anteriores habían identificado erróneamente los RiPP fúngicos como péptidos no ribosomales y sabían poco sobre cómo producen los hongos estas moléculas. Según los investigadores, la síntesis de estos compuestos es complicada. Para encontrar más RiPP en los hongos, examinaron primero una docena de cepas de Aspergillus, que según investigaciones anteriores podrían contener más de estas sustancias químicas. Al comparar las sustancias químicas producidas por estas cepas con los componentes conocidos de las RiPP, identificaron el A. flavus como un candidato prometedor para futuras investigaciones.
Los análisis genéticos apuntaron a una proteína específica de A. flavus como fuente de RiPPs fúngicas. Cuando los investigadores desactivaron los genes que producen esta proteína, también desaparecieron los marcadores químicos que indicaban la presencia de RiPPs. Este novedoso enfoque -que combina información metabólica y genética- no sólo ha identificado la fuente de RiPPs fúngicas en A. flavus, sino que también podría utilizarse para encontrar otras RiPPs fúngicas en el futuro.
Fuerte efecto contra la leucemia
Tras purificar cuatro RiPP diferentes, los científicos se dieron cuenta de que las moléculas tenían una estructura única de anillos entrelazados. Bautizaron estas moléculas, que aún no se habían descrito, con el nombre del hongo en el que se encontraron: Asperigimicinas. Incluso sin modificarlas, las asperigimicinas mostraron potencial médico en combinación con células cancerosas humanas: dos de las cuatro variantes tuvieron un fuerte efecto contra las células leucémicas.
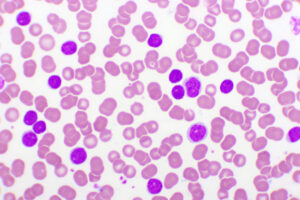
Otra variante, a la que los investigadores añadieron un lípido (molécula grasa) que también contiene la jalea real de la que se alimentan las abejas durante la fase de desarrollo, mostró un efecto tan bueno como la citarabina y la daunorrubicina, dos fármacos aprobados por la FDA que se utilizan para tratar la leucemia desde hace décadas.
Instrumento para el desarrollo de fármacos
Para entender por qué los lípidos aumentan la eficacia de las asperigimicinas, los investigadores activaron y desactivaron selectivamente determinados genes de las células leucémicas. Un gen, el SLC46A3, resultó ser crucial para que las asperigimicinas penetraran en las células leucémicas en cantidades suficientes. Este gen ayuda a excretar sustancias de los lisosomas, las diminutas vesículas que recogen las sustancias extrañas que entran en las células humanas.
Al igual que las asperigimicinas, estas sustancias químicas tienen propiedades medicinales -desde el año 2000 se han aprobado casi dos docenas de péptidos cíclicos para el tratamiento de enfermedades tan diversas como el cáncer y el lupus-, pero muchas de ellas necesitan ser modificadas para penetrar en las células en cantidades suficientes. «Ahora que sabemos que los lípidos pueden influir en el transporte de sustancias químicas a las células a través de este gen, disponemos de otra herramienta para el desarrollo de fármacos», afirma Nie.
Posiblemente algún día ensayos clínicos en humanos
Mediante experimentos adicionales, los investigadores descubrieron que las asperigimicinas probablemente interfieren en el proceso de división celular. Sorprendentemente, los compuestos apenas tuvieron efecto en las células de cáncer de mama, hígado o pulmón -o en una serie de bacterias y hongos-, lo que, según los expertos, sugiere que los efectos perturbadores de las asperigimicinas son específicos de determinados tipos celulares, algo crucial para futuros fármacos.
Además de demostrar el potencial medicinal de las asperigimicinas, los investigadores identificaron grupos de genes similares en otros hongos, lo que sugiere que podrían descubrirse aún más RiPPS en los hongos. El siguiente paso es probar las asperigimicinas en modelos animales con la esperanza de pasar algún día a ensayos clínicos en humanos.


